Răspunsul tuberculozei la chimioterapicele...
Transcript of Răspunsul tuberculozei la chimioterapicele...

Răspunsul tuberculozei la
chimioterapicele antituberculoase
Stud. Radu Daniela-Noela ¹, Stud. Răboj Lavinia ¹, Stud. Stuparu Gheorghe Cosmin ¹,
Dr. Stoica Lavinia Alexandra ²
¹ Universitatea de Medicină şi Farmacie „Carol Davila” Bucureşti, ² Institutul de Pneumologie „Marius Nasta”, Bucureşti
Rezumat: Tuberculoza este o boală infecțioasă multisistemică ce rămâne o problemă majoră de sănătate publică atât la nivelul
României, cât și la nivel global, în ciuda faptului că există scheme de tratament cu rate mari de succes. Acest studiu analizează
corelațiile existente între variabilele ce țin de pacienți și evoluția si răspunsul acestora la schemele de tratament cu
tuberculostatice, urmărind incidența reacțiilor adverse și abordarea acestora. Au fost analizate retrospectiv foile de observație a
60 de pacienți internați în Institutul de Pneumologie “Marius Nasta” București în perioada martie-august 2015, cu suspiciunea de
tuberculoză pulmonară sau extrapulmonară. Rezultatele obținute au fost în concordanță cu cele înregistrate în alte studii. Vârsta
medie a pacienților incluși a fost de 48 de ani, cu predominanța sexului masculin și a fumătorilor; simptomatologia a fost
reprezentată predominant de tuse și dispnee, iar diagnosticul confirmat, în principal, prin examenul bacteriologic al sputei sau
aspiratului bronșic. Majoritatea pacienților (76.67%) au urmat regimul de tratament I, 6.67%- regimul II, iar 13.33%- regim
individualizat, existând două cazuri fără administrarea niciunui tratament. Reacțiile adverse s-au manifestat în 45% din cazuri,
mai frecvent la pacienții de sex feminin sau cu vârste peste 60 de ani. Reacțiile adverse cele mai întâlnite au fost cele de tip
gastro-intestinal. Prezența comorbidităților, îndeosebi a etilismului cronic, hepatitei cronice virale B sau C și insuficienței renale
cronice, a predispus la apariția reacțiilor adverse. Evoluția pacienților sub tratament tuberculostatic strict supravegheat pe durata
internării a fost consemnată ca favorabilă sau lent favorabilă în proporție de 94,83%, ridicându-se premisele unei evoluții
asemănătoare și după externare. În concluzie, medicamentele antituberculoase au o rată mare de eficiență, dar și o toxicitate
relativă, influențată de vârsta, sexul și comorbiditățile asociate ale pacientului, reunite sub caracterul de factori de risc ce
predispun la reacții adverse.
Cuvinte cheie: tuberculoză, TSS, reacții adverse, PNCT
Abstract: Tuberculosis is a multisystemic infectious disease that persists as a major public health problem not only in Romania,
but also globally, despite the fact that there are treatment algorithms with great success rates. The study analyses the correlations
between the variables of the patients and their evolution and response to the tuberculostatic treatment, following the incidence of
adverse reactions and their management. The files of 60 patients admitted under the suspicion of pulmonary or extrapulmonary
tuberculosis to “Marius Nasta” Institute of Pulmonology during the period of March to August 2015 were studied retrospectively.
The obtained results were similar to those of other studies. The median age of the included patients was 48 years, with a majority
of males and smokers; the most frequent symptoms were cough and dyspnea and the diagnosis was mainly confirmed by the
bacteriologic exam of sputum or broncho-alveolar lavage. The majority of the patients (76.67%) followed the first regime of
treatment, 6,67%, the second regime and 13,33%, individualised regime, with two cases that did not follow any treatment.
Adverse effects appeared in 45% of the cases, mainly in female patients or patients older than sixty years. The most frequent
adverse reactions affected the gastro-intestinal system. The presence of comorbidities, particularly chronic alcohol abuse, chronic
virus B or C hepatitis and chronic renal failure predisposed to the emergence of adverse reactions. The evolution of the patients
under directly observed tuberculostatic treatment during hospitalization was noted as favorable or slow favorable in proportion of
94,83%, presuming a similar evolution also after discharge. In conclusion, not only the antituberculosis treatment has a great rate
of efficiency, but also relative toxicity, influenced by the age, sex and associated comorbidities of the patient, considered risk
factors for drugs-related side effects.
Key words: Tuberculosis, DOT, adverse reactions, PNCT

Introducere
Tuberculoza este o infecție bacteriană specifică, larg răspândită, determinată de agenți etiologici
aparținând „complexului Mycobacterium tuberculosis” ce include speciile M. tuberculosis, M. bovis și M.
africanum; poate afecta persoane de orice vârstă și orice parte a corpului, dar, în mod tipic, se localizează
la nivelul plămânilor[1]
. Transmiterea se face pe cale aeriană, sursa de infecție fiind reprezentată de o
persoană cu tuberculoză pulmonară; gradul de contagiozitate este însă determinat de densitatea bacililor
acid-alcool rezistenți în spută și de frecvența tusei[2]
. În circa 80% din cazuri, tuberculoza se localizează la
nivel pulmonar, dar poate lua și formă extrapulmonară, afectând cel mai frecvent pleura, ganglionii
limfatici, sistemul osteo-articular, căile genito-urinare sau sistemul gastro-intestinal. Este caracterizată,
din punct de vedere morfopatologic, de o pronunțată diversitate lezională, cu caracter infiltrativ, exsudativ
sau cu prezența necrozei de cazeificare. De asemenea, se particularizează prin relația existentă între
infecție și manifestarea propriu-zisă a bolii; astfel, dintre subiecții infectați, 80-90% nu vor manifesta
niciodată simptomatologia tipică tuberculozei, în ceea ce privește restul de 10-20% dintre persoanele
infectate dezvoltarea bolii făcându-se pe seama mecanismelor de imunitate compromise. Boala prezintă o
evoluție cronică și o fatalitate semnificativă în cazul în care este netratată sau tratată incorect[1]
.
Există dovezi ale prezenței tuberculozei la om încă din perioada Egiptului antic, datând deci de cel puțin
3000 de ani. Interesul marcat al cercetătorilor secolului al XIX-lea privind această patologie a dus la
progrese importante în cunoașterea bolii; astfel, Laennec a realizat caracterizarea clinică a tuberculozei,
Villemin a demonstrat caracterul transmisibil, iar Robert Koch a identificat agentul etiologic, realizând
premisele diagnosticului bacteriologic al tuberculozei. În secolul al XX-lea accentul a fost pus pe
cercetarea modalităților terapeutice, ceea ce s-a concretizat în apariția vaccinului BCG și descoperirea
antituberculoaselor de primă linie: streptomicina, izoniazida, etambutolul, rifampicina și pirazinamida[2]
.
În ciuda faptului că există scheme de tratament eficiente (rata de succes raportată de Organizația
Mondială a Sănătății (OMS) în 2014 este de peste 85%[3]
), tuberculoza rămâne o problemă de sănătate
majoră la nivel global, estimându-se un numar de 9 milioane de cazuri noi și 1,5 milioane de decese în
2013[3]
. Conform statisticii OMS din anul 2013, România se află printre țările cu nivel de morbiditate
crescut, exprimat printr-o incidență de 87‰₀₀ și o prevalență de 123‰₀₀[3]. Mortalitatea este estimată la
5,4‰₀₀[3], în scădere, datorită implementării unui plan de sănătate publică, Programul Național de Control
al Tuberculozei, ce are ca obiectiv prevenția, diagnosticarea precoce și tratamentul complet al
tuberculozei.
Scopul acestui studiu este să analizeze gradul de complianță și de răspuns la schemele de tratament cu
tuberculostatice (regimurile I, II sau individualizat), în funcție de vârstă, sex, mediu de proveniență
(rural/urban), comorbidități asociate, pe un lot de 60 de pacienți cu tuberculoză pulmonară sau
extrapulmonară, cazuri confirmate bacteriologic și/sau histopatologic, care au beneficiat de internare și
tratament strict supravegheat, în general pe o perioadă de cel puțin 30 de zile, în cadrul Institutului de
Pneumologie „Marius Nasta”. De asemenea, se monitorizează incidența reacțiilor adverse ale
chimioterapicelor antituberculoase la nivel digestiv, cutanat, neurologic, hematologic, renal. Studiul se
rezumă strict la pacienții cu tuberculoză cu antibiogramă sensibilă la chimioterapicele de prima intenție,
fără a fi luate în calcul cazurile de tuberculoză multidrog rezistentă.

Materiale și metode
Pentru realizarea acestui studiu s-a folosit un lot de 60 de pacienți cu suspiciune de tuberculoză
pulmonară sau extrapulmonară. Dintre aceștia, 45 de cazuri au fost confirmate prin microscopie,
citologie, histopatologie sau test genetic, restul neputând fi confirmate astfel, decizia diagnostică fiind
luată pe baza semnelor, simptomelor clinice și a modificarilor radiologice, cu mențiunea că există un caz
infirmat.
Studiul este cantitativ retrospectiv, pacienții fiind selectați din arhiva Institutului de Pneumologie “Marius
Nasta” București, internați în perioada martie-august a anului curent.
În vederea îndeplinirii studiului s-a obținut consimțământul pacienților de a fi investigați și de a li se
utiliza datele personale. Pacienții au fost informați și instruiți în legătură cu procedurile la care au fost
supuși, incluzând beneficiile și riscurile acestora.
S-au luat în considerare vârsta, sexul, proveniența (mediu rural/urban) pacienților incluși în studiu,
precum și durata de spitalizare. Pacienții au fost grupați în funcție de comportamentele la risc
(fumător/fost fumător) și expunerea la noxe respiratorii.
S-a consemnat simptomatologia la internare, specifică pentru patologia sistemului respirator: tuse seacă
sau productivă, dispnee, inapetență, scădere ponderală, junghi toracic, astenie fizică, febră, transpirații,
fatigabilitate și hemoptizii.
Investigațiile paraclinice care au confirmat diagnosticul au fost examenul microscopic bacteriologic și
culturile pe mediu lichid ale sputei, aspiratului bronșic și lichidului pleural. Analizele de laborator,
probele funcționale respiratorii, radiografia pulmonară în incidență postero-anterioară și profil și
tomografia computerizată au fost și ele folosite pentru obiectivarea afectării pluriorganice. O parte dintre
pacienți au necesitat investigații invazive precum bronhoscopie și recoltare aspirat bronșic, puncție și
biopsie pleurală, recoltare lichid pleural pentru evaluare bacteriologică, citologică și biochimică, și
biopsie pulmonară.
S-a urmărit cu atenție tipul de regim de tratament tuberculostatic administrat, dozele prescrise în funcție
de comorbiditățile asociate, rezistența la anumite chimioterapice și medicamentele folosite în
individualizare. O mare importanță s-a acordat reacțiilor adverse (digestive, alergice, hepatice,
neurosenzoriale, psihiatrice, renale, hematologice) apărute în contextul administrării tratamentului sub
supraveghere, precum și necesității interferării cu schema de tratament.
Pentru evaluarea eficienței tratamentului, s-a efectuat diagnosticul microscopic al produselor patologice
(spută/aspirat bronșic) la o lună de la debutul tratamentului, notându-se absența bacililor acid-alcool
rezistenți. De asemenea, s-a urmărit starea pacienților în momentul externării și s-a notat modalitatea de
continuare a tratamentului strict supravegheat efectuat conform Programului Național de Control al
Tuberculozei.
Baza de date obținută în urma analizării atente a dosarelor de internare ale celor 60 de pacienți a fost
prelucrată cu ajutorul programului Microsoft Office Excel 2010.

Rezultate
Din totalul de 60 de pacienţi incluşi în studiu, 36 sunt bărbaţi (60%), iar 24 femei (40%), cu vârste
cuprinse între 20 şi 85 de ani, vârsta medie fiind de 48 de ani. Am analizat repartiţia pe grupe de vârstă şi
sex a subiecţilor studiaţi (Figura 1). În ceea ce priveşte mediul de provenienţă, 41 de pacienţi locuiesc în
mediul urban (68,3%) şi 19 în mediul rural (31,7%). Durata de spitalizare medie a fost de 37,4 zile, cu un
minim de 8 zile şi un maxim de 119 zile.
Figura 1
În ceea ce priveşte expunerea la particule inhalatorii, 34 de pacienţi sunt fumători sau foşti fumători
(56,67%), 26 nefumători (43,33%), iar 17 pacienţi au fost expuşi la noxe profesionale (28,33%). S-a
constatat că 11 pacienţi au dublă expunere, atât la fumul de ţigară cât şi la noxele ocupaţionale, dar şi
faptul că există 20 de pacienţi ce neagă contactul cu noxe şi particule inhalatorii.
Referitor la simptomatologia la internare se constată că cele mai frecvente simptome sunt tusea seacă sau
productivă (apărută la 40 de pacienţi) şi dispneea la eforturi mari/moderate/mici (la 36 de pacienţi),
asocierea celor două acuze fiind întâlnită la 26 de pacienţi. Scăderea ponderală (23 de cazuri), junghiul
toracic (22 de cazuri) şi astenia fizică (21 de cazuri) sunt următoarele simptome de prezentare la internare
urmate, ca frecvenţă, de simptome precum inapetenţă (15 cazuri), febră (14 cazuri), transpiraţii (12
cazuri), fatigabilitate (11 cazuri) şi hemoptizii (7 cazuri). Simptomele şi rata lor procentuală de
manifestare în cadrul lotului de pacienţi sunt prezentate în Figura 2.
6
2
7
12
7
14
4
8
0
2
4
6
8
10
12
14
Nu
mă
r p
ac
ien
ți
15-24 ani 25-44 ani 45-64 ani >=65 ani
Vârsta
Repartiția pe grupe de vârstă și sex a subiecților studiați
Femei
Bărbați

Figura 2
Diagnosticul final pentru cei 60 de pacienţi la care s-a ridicat suspiciunea de tuberculoză pulmonară sau
extrapulmonară a fost stabilit după cum urmează:
41 de pacienţi (68,33%)- tuberculoză pulmonară;
9 pacienţi (15%)- tuberculoză pulmonară asociată cu afectare extrapulmonară;
9 pacienţi (15%)- tuberculoză extrapulmonară exclusiv.
A existat un caz care, datorită unui examen bacteriologic pozitiv (frotiu din spută negativ, dar culturi din
spută pozitive), a fost considerat iniţial tuberculoză pulmonară, pentru ca, ulterior, în lipsa leziunilor
pulmonare sugestive pentru această patologie, diagnosticul să fie infirmat. Cei 9 pacienţi cu patologie atât
pulmonară, cât şi extrapulmonară au asociat tuberculoză pleurală (5 cazuri), tuberculoză laringiană (un
caz), tuberculoză peritoneală (un caz), tuberculoză genito-urinară (un caz) şi tuberculoză anorectală (un
caz). În cazul celor 9 pacienţi diagnosticaţi per primam cu tuberculoză extrapulmonară, structurile
afectate au fost fie pleura (7 cazuri), fie ganglionii limfatici (2 cazuri).
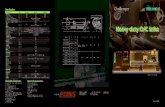
Formele de tuberculoză pulmonară întâlnite au fost variate, diagnosticul imagistic ajutând la stabilirea
stadiului morfopatologic (infiltrativ-nodulară, infiltrativ-ulcerată, cazeos-circumscrisă, cazeos-ulcerată,
fibro-cazeoasă, cazeos-cavitară, cavitară, miliară) şi a regiunii pulmonare afectate. Două dintre cele mai
frecvente forme întâlnite sunt ilustrate în Figura 3.
Simptomatologia la internare
66.67%
60.00%
35%
25%
23.33%
20%
18.33% 11.67%
36.67% 38.33%
tuse
dispnee
scadere ponderală
junghi toracic
astenie fizică
inapetență
febră
transpirații
fatigabilitate
hemoptizii

Figura 3
Având în vedere că nu toate cazurile au putut fi confirmate prin diagnosticul bacteriologic al sputei, o
parte dintre pacienţi au necesitat investigaţii invazive precum bronhoscopie şi recoltare aspirat bronşic (30
de pacienţi), puncţie şi biopsie pleurală (10 pacienţi), recoltare lichid pleural (13 pacienţi), pentru
evaluare bacteriologică, citologică şi biochimică, sau biopsie pulmonară (3 pacienţi).
Diagnosticul a fost confirmat prin investigaţii paraclinice variate:
pentru 25 de pacienţi, prin examen microscopic bacteriologic al sputei sau aspiratului bronşic;
pentru 4 pacienţi, prin culturi pe mediu lichid ale produselor patologice (în absenţa bacililor acid-
alcool rezistenţi la examenul microscopic);
în 14 cazuri, suspiciunea a fost confirmată prin diagnosticul histopatologic al probelor obţinute în
urma biopsiei: fragmente pulmonare, pleurale, ganglionare, din corzile vocale (tuberculoză
laringiană) sau din formaţiuni tumorale, fie gastrică (tuberculoză peritoneală), fie de la nivelul
canalului anal (tuberculoză anorectală);
pentru 3 pacienţi, diagnosticul s-a stabilit prin izolarea genetică a Mycobacterium Tuberculosis
din produsele patologice (prin teste genetice GeneXpert, LPA).
Chiar dacă au fost utilizate multiple posibilităţi de diagnosticare, în 16 cazuri nu s-a putut realiza izolarea
germenului patogen, iar decizia diagnostică şi terapeutică a fost luată pe baza semnelor şi simptomelor
clinice şi a modificărilor radiologice.
Pacienţii incluşi în studiu au urmat unul din cele trei regimuri de tratament:
46 de pacienţi (76,67%) au urmat regimul de tratament I (Izoniazidă 5-10 mg/kg corp,
Rifampicină 10 mg/kg corp, Pirazinamidă 20-30 mg/kg corp, Etambutol 15-25 mg/kg corp),
dintre care 12 pacienţi (26,09%) au primit doze ajustate în funcţie de greutatea corporală sau
comorbidităţi;
4 pacienţi (6,67%) au urmat regimul de tratament II (Izoniazidă 5-10 mg/kg corp, Rifampicină
10 mg/kg corp, Pirazinamidă 20-30 mg/kg corp, Etambutol 15-25 mg/kg corp), fiind cazuri de
tuberculoză recidivată;

8 pacienţi (13,33%) au urmat un regim de tratament individualizat, medicamentele adăugate fiind,
în ordinea frecvenţei utilizării, următoarele: Streptomicină (16,67%), Chinolone (8,33%),
Protionamidă (3,33%) şi Cicloserină (1,67%).
De menţionat că au existat 2 pacienţi care nu au primit tratament tuberculostatic la momentul internării:
un caz de tuberculoză a fost infirmat, iar pentru al doilea pacient a fost recomandată iniţierea
tratamentului specific într-un alt serviciu de pneumoftiziologie.
Distribuţia pacienţilor în funcţie de regimurile de tratament urmate este reprezentată în Figura 4.
Figura 4
Cele mai utilizate medicamente antituberculoase folosite în schemele de tratament au fost, în proporţii
egale, Izoniazida şi Rifampicina, în 55 de cazuri (91,67%), urmate de Etambutol, utilizat în 54 de cazuri
(90%), şi Pirazinamidă, administrată la 53 de pacienţi (88,33%). Distribuţia pacienţilor în funcţie de
tuberculostaticele utilizate este reprezentată în Figura 5.
Figura 5

Reacţii adverse ale tratamentului tuberculostatic au fost prezente la 27 dintre cei 60 de pacienţi (45%).
Vârsta medie a pacienţilor care au prezentat reacţii adverse a fost de 50 de ani, uşor mai mare faţă de
vârstă medie generală de 48 de ani. S-a constatat faptul că 55% dintre pacienţii cu vârste peste 60 de ani
au manifestat reacţii adverse, faţă de numai 40% dintre pacienţii cu vârste mai mici de 60 de ani.
Incidenţa pe sexe a relevat o predispoziţie a sexului feminin de a dezvolta reacţii adverse (62,50%), pe
când la sexul masculin incidenţa a fost de 33,33%. În acelaşi context s-a observat faptul că 66,66% din
pacienţii ce au manifestat reacţii adverse de tip hepatic sunt femei, iar 33,33% sunt bărbaţi.
S-a observat o corelaţie importantă şi între prezenţa comorbidităților şi apariţia efectelor adverse. Astfel,
din cei 35 de pacienţi cu antecedente personale patologice, 19 au prezentat reacţii adverse la tratamentul
cu tuberculostatice (54,28%), în comparaţie cu numai 8 pacienţi din cei 23 fără comorbidităţi (34,78%).
S-a constatat faptul că în grupul celor 27 de pacienţi care au manifestat reacţii adverse există 4 cazuri de
etilism cronic, 2 cazuri de hepatită cronică cu virusuri hepatitice (B sau C), dintre care unul asociat cu
dependenţă de alcool, un pacient cu insuficiență renală cronică stadiul III şi un pacient ce prezintă atât
hepatită cronică cu virus hepatitic C, cât şi insuficienţă renală cronică.
Cele mai frecvente reacţii adverse au fost cele gastro-intestinale (întâlnite la 20 de pacienţi). S-au
înregistrat 8 cazuri de diaree, pentru unul singur fiind confirmată infecţia cu Clostridium difficile (prin
examen coproparazitologic). Reacţiile adverse hepatice au fost consemnate în 9 cazuri, manifestându-se
prin creşterea simptomatică sau asimptomatică a transaminazelor. Alte reacţii adverse gastro-intestinale
au fost, în ordinea frecvenţei: greaţă, vărsături sau disfagie.
Au fost depistaţi 7 pacienţi cu hiperuricemie (pentru care s-a administrat alopurinol) ca reacţie adversă la
administrarea Pirazinamidei. Reacţii adverse alergice au fost depistate la 4 pacienţi şi au constat în erupţii
eritematoase şi prurit. Tot în număr de 4 cazuri s-au întâlnit şi reacţiile neurosenzoriale, dintre care 2
cazuri au prezentat sindrom vertiginos, însoţit sau nu de cefalee.
Alte reacţii adverse în urma administrării tratamentului antituberculos au fost: psihiatrice (3 cazuri) din
care reţinem depresia şi anxietatea, 2 cazuri de purpură trombocitopenică şi un singur caz de insuficiență
renală acută. Reacţiile adverse şi rata procentuală de apariţie sunt prezentate în Figura 6.
Figura 6
Reacții adverse
20.93%
18.60%
16.28%
18.60%
9.30%
9.30%6.98% Reacții adverse hepatice
Diaree
Greață
Manifestări hematologice
Reacții adverse neurosenzoriale
Reacții adverse alergice
Reacții adverse psihiatrice

Reacţiile adverse apărute pe durata spitalizării în cazul a 14 pacienţi au determinat interferarea cu schema
de tratament. Astfel:
11 pacienţi au întrerupt întregul tratament pentru perioade variind de la o zi până la 25 de zile,
acesta fiind ulterior reluat, fără apariţia altor reacţii adverse;
2 pacienţi au întrerupt un singur medicament (Izoniazida sau Pirazinamida), în urma apariţiei
reacţiilor adverse de tip alergic, hiperuricemie sau sindrom maniacal, tratamentul fiind reluat
după circa 3 zile, fără apariţia altor reacţii adverse;
s-a înregistrat un singur caz de întrerupere definitivă a unui medicament (Izoniazida), datorită
apariţiei rezistenţei la acest tuberculostatic, obiectivată prin rezultatul antibiogramei.
Pentru evaluarea eficienţei tratamentului, s-a efectuat diagnosticul microscopic al produselor patologice
(spută/aspirat bronşic) la o lună de la debutul tratamentului. Din cei 25 de pacienţi consemnaţi iniţial cu
examen microscopic pozitiv al probelor recoltate, în cazul a 12 pacienţi (48%) reexaminarea microscopică
la o lună a notat absenţa bacililor acid-alcool rezistenţi.
În ceea ce priveşte evoluţia sub tratament, aceasta a fost stabilită ca fiind favorabilă în cazul a 28 de
pacienţi (48,27%), lent favorabilă pentru 27 de pacienţi (46,55%) şi nefavorabilă pentru 3 pacienţi
(5,17%) (reamintim faptul că 2 pacienţi incluşi în studiu nu au primit tratament tuberculostatic). Evoluţia
sub tratament s-a corelat şi cu prezenţa sau absenţa comorbidităților. Astfel, 52,17% din pacienţii fără
antecedente personale patologice au avut o evoluţie favorabilă, pe când 45,71% din cei cu comorbidităţi
au avut o evoluţie favorabilă.
Referitor la modalitatea de continuare a tratamentului strict supravegheat, efectuat conform Programului
Naţional de Control al Tuberculozei, majoritatea pacienţilor au fost externaţi cu recomandare de
continuare a tratamentului antituberculos prin dispensarul teritorial (86,66%), notându-se 2 cazuri de
externare cu recomandare de continuare a tratamentului în regim de sanatoriu.
Discuții
Institutul de Pneumologie “Marius Nasta” este centru terțiar de tratament, având o bogată experiență în
managementul pacientului bolnav de tuberculoză (posibilități multiple de diagnosticare) cât și un număr
foarte mare de pacienți, dintr-un spațiu geografic întins. Acest fapt a conferit heterogenitate lotului de
pacienți studiat în ceea ce privește toate variabile pe care ne-am propus să le urmărim.
Vârsta a reprezentat un criteriu de analiză a incidenței reacțiilor adverse. Astfel, vârsta medie mai mare a
pacienților ce au manifestat reacții adverse, cât și frecvența crescută la grupul de vârstă de peste 60 de ani
sunt în conformitate cu Baghaei et al. care demonstrează că vârsta peste 60 de ani poate fi considerată
factor de risc în apariția reacțiilor adverse[4]
. Acest fapt se datorează unei rate a metabolismului bazal mai
redusă la vârstnici, pe seama unei activități enzimatice diminuate, a unui clearance hepatic încetinit și a
disponibilității reduse a cofactorilor endogeni[5]
.
De asemenea, incidența crescută a reacțiilor adverse la sexul feminin față de cel masculin sugerează un
fapt confirmat și de Yee D et al., și anume, predispoziția crescută a sexului feminin de a manifesta reacții
adverse[6]
. În plus, am constatat că sexul masculin este factor protector împotriva hepatotoxicității[7]
(fapt

evidențiat și de Lee AM et al.), posibil datorită faptului că activitatea androgenică crește activitatea
enzimelor microzomale hepatice, medicamentele fiind metabolizate mai eficient[5]
.
S-a observat că pacienții cu comorbidități sunt mai predispuși la apariția de reacții adverse decât pacienții
fără antecedente personale patologice, fapt constatat și de Kim SY et al., într-un studiu despre efectele
adverse ale tuberculostaticelor la vârstnici[8]
. În cadrul lotului de pacienți ce au prezentat reacții adverse
au fost notate cazuri de etilism cronic, hepatită cronică cu virusuri hepatitice B sau C și insuficiență
renală, observații sugestive în contextul în care aceste patologii au fost citate ca factori de risc pentru
apariția de reacții adverse[9-13]
.
Din cei 11 pacienți cunoscuți cu etilism cronic incluși în studiu, evoluția a fost favorabilă pentru 45,45%
din ei, lent favorabilă în aceeași măsură și nefavorabilă în cazul unui pacient (9,09%) (acesta din urmă
având asociată și tuberculoză anorectală). Pentru 7 pacienți nu s-au raportat reacții adverse (63,63%), iar
în cazul celorlalți 4 pacienți s-au consemnat manifestări adverse de tip gastro-intestinal, neurosenzorial,
cutanat sau hiperuricemie. Nu s-a observat creșterea transaminazelor în cazul niciunuia dintre acești
pacienți, iar tratamentul a fost întrerupt și reluat la scurt timp doar în cazul unui singur pacient (acesta
manifestând prurit intens, cefalee și vertij).
În cazul celor 3 pacienți cu hepatită cronică, evoluția a fost lent favorabilă; unul dintre ei nu a asociat
reacții adverse, însă ceilalți doi au manifestat efecte adverse. Astfel, un caz a asociat creșterea
transaminazelor și diaree, ce a determinat întreruperea și reluarea tratamentului după 4 zile, iar celălalt
pacient a asociat diaree, sindrom vertiginos, hiperuricemie și purpură trombocitopenică (ca reacție
adversă la rifampicină), fiind necesară oprirea în două rânduri a tratamentului și individualizarea sa
(întreruperea administrării de rifampicină și introducerea streptomicinei).
Două din cele 3 cazuri de insuficiență renală cronică au avut o evoluție favorabilă, fără apariția reacțiilor
adverse. Pe de altă parte, în cel de-al treilea caz s-a impus oprirea inițială a tratamentului pentru 25 de zile
din cauza decompensării insuficienței renale și apariției sindromului diareic (confirmându-se prin
examenul coproparazitologic infecția cu Clostridium difficile și administrându-se tratament antibiotic
specific cu Metronidazol asociat cu Vancomicină). Ulterior, tratamentul a fost sistat și reluat de două ori
din cauza simptomatologiei determinate de hemoragia digestivă superioară (hematemeză în jet, melenă)
pe seama unei afectări de tip ulceros a porțiunii eso-gastro-duodenale, tratată prin hemostază endoscopică.
Pacientul care asociază hepatită cronică cu virus hepatitic C și insuficiență renală a avut o evoluție
favorabilă, fără apariția reacțiilor adverse. Tratamentul strict supravegheat reprezintă un element esențial
al succesului terapeutic. Obiective precum îmbunătățirea aderenței la tratament și prevenirea
chimiorezistenței s-au realizat prin utilizarea comprimatelor ce conțin doze fixe de antituberculoase și,
mai ales, prin terapia sub directă observare (DOT - directly observed therapy). DOT reprezintă
modalitatea de elecție pentru administrarea tratamentului antituberculos și presupune supravegherea
momentului ingestiei medicamentelor de către personal medical sau oricare altă persoană preferată de
pacient, dar responsabilizată față de medicul curant[14]
.
Tratamentul pacienților s-a realizat conform ghidurilor de tratament din Programul Național de Control al
Tuberculozei, în 3 regimuri: regim I, regim II și regim individualizat, dintre care cel mai utilizat a fost
regimul I în proporție de 76,67%. Tratamentul a fost inițiat pe durata spitalizării și continuat ulterior prin
dispensar teritorial sau în regim de sanatoriu.

Tratamentul s-a realizat cu chimioterapice majore, precum Izoniazida (HIN) și Rifampicina (RMP), și
chimioterapice de asociere: Pirazinamida (PZM), Etambutolul (EMB) și Streptomicina (SM), iar pentru
regimul individualizat s-au adăugat medicamente din clasa chinolonelor, Cicloserina sau Protionamida.
Reacțiile adverse în urma tratamentului antituberculos au fost prezente la 45,00% din pacienți, dintre
acestea cele mai frecvente fiind reacțiile gastro-intestinale (33,33% din subiecți): diaree, creșterea
transaminazelor, greață, vărsături, disfagie. Acest rezultat se află în concordanță cu alte studii care citează
manifestările gastro-intestinale ca fiind cele mai frecvente efecte adverse ale tuberculostaticelor[15,16]
. De
subliniat incidența crescută a diareei, întâlnindu-se în 9 cazuri, fapt ce a dus la o evoluție mai frecvent lent
favorabilă, cu creșterea duratei de spitalizare (în medie, cu 12 zile mai mult). De asemenea, în 6 din cele 9
cazuri a fost necesară întreruperea temporară a tratamentului pentru o durată medie de 9 zile, iar pentru 7
pacienți s-a administrat tratament antibiotic specific cu Metronidazol asociat cu Vancomicină (6 cazuri) și
Furazolidon (1 caz). În ceea ce privește cauzele apariției diareei, dintre cele 9 cazuri de diaree, un singur
caz a fost diagnosticat ca fiind infecție cu Clostridium difficile, cu mențiunea că nu au existat posibilități
de analiză a coproculturii la toți pacienții. Deși infecția cu Clostridium difficile (cea mai comună cauză a
diareei intraspitalicești) este de cele mai multe ori precedată de tratamentul antibiotic cu fluorochinolone,
cefalosporine, peniciline cu spectru larg și clindamicină, și mai puțin de antibioticele folosite în
tratamentul tuberculozei[17]
, studiul lui Lee YM et al. identifică o incidență de 2,83/1000 adulți tratați cu
antituberculoase, demonstrând totodată că nu există o diferență semnificativă în ceea ce privește durata
până la vindecare a sindromului infecțios diareic între pacienții cărora li s-a întrerupt tratamentul și cei
care l-au continuat[18]
. De remarcat că vârsta medie a pacienților cu diaree a fost de 54 ani (cu 6 ani mai
mare decât vârsta medie generală) și că 7 din 9 cazuri au prezentat comorbidități, fapt ce sugerează
susceptibilitatea crescută de a dezvolta reacții adverse gastro-intestinale a pacienților mai în vârstă și cu
comorbidități.
Izoniazida, notată de către Castro et al. ca fiind cauza principală de hepatotoxicitate[19]
, este și în studiul
nostru responsabilă pentru afectare hepatică. Astfel, în cazul a doi pacienți la care s-a înregistrat o creștere
a transaminazelor de peste 5 ori valoarea normală, s-a impus întreruperea tratamentului pentru perioade
variabile de timp și reluarea sa ulterioară. Un alt efect advers al tratamentului cu Izoniazidă, nevrita
periferică, manifestată prin parestezii ale extremităților, apare pe fondul hipovitaminozei B6, fiind
utilizată profilaxia cu piridoxină la pacienții cu risc crescut[20, 21]
. În studiul nostru, un singur pacient a
prezentat nevrită periferică, același pacient dezvoltând, pe lângă creșterea asimptomatică a
transaminazelor, manifestări eritemato-pruriginoase la nivelul membrelor superioare, precum și reacții
psihiatrice.
Rifampicina dă reacții adverse precum purpura trombocitopenică, anemia hemolitică și insuficiența renală
acută prin mecanism de hipersensibilizare, având ca rezultat inițial necroza tubulară acută sau nefrita
interstițială. Pe parcursul spitalizării pacienților aflați în studiu, doar purpura trombocitopenică și
insuficiența renală acută au fost întâlnite ca posibile manifestări adverse la tratamentul cu rifampicină.
Pirazinamida prezintă ca reacții adverse caracteristice erupții cutanate, hiperuricemie și reacții gastro-
intestinale. În studiul nostru, hiperuricemia a fost cel mai frecvent întâlnit efect advers, dar și una dintre
cele mai frecvente reacții adverse apărute în general. Există și alte studii ce confirmă rata mare de apariție
a hiperuricemiei ca efect advers la administrarea de pirazinamidă cum este cel derulat de Solangi et al. [22]
. Pentru combaterea hiperuricemiei s-a administrat tratament uricozuric (alopurinol).

În ciuda frecvenței crescute a reacțiilor adverse (45%) și a unui număr relativ mare de cazuri de
întrerupere parțială sau a întregului tratament (23,33% din pacienți), evoluția pacienților a fost favorabilă
sau lent favorabilă în proporție de 94,83%, înregistrându-se doar 3 cazuri de evoluție nefavorabilă. S-a
observat că vârsta tânără, sexul masculin și lipsa comorbidităților sunt factori pozitivi pentru o evoluție
favorabilă. În ceea ce privește comportamentele la risc, este cunoscut că etilismul cronic favorizează
reacțiile adverse hepatice și neurologice. De asemenea, acest comportament atrage după sine un status
nutrițional sărac, afectare hepatică de diverse grade, precum și tulburări psihice asociate, care interferă cu
respectarea tratamentului, ducând la o evoluție nefavorabilă[1]
. Cu toate acestea, consumatorii cronici de
alcool din studiu au avut o evoluție similară populației generale, iar fumatul a constituit un factor de
prognostic neglijabil, fumătorii având o evoluție favorabilă în proporție de 44,12% față de 50% la
nefumători. Un alt aspect important cu privire la evoluția pacienților bolnavi de tuberculoză aflați sub
tratament îl constituie regimul igieno-dietetic. Bolnavul ce suferă de tuberculoză activă, contagioasă,
trebuie să evite locurile aglomerate, precum mijloacele de transport public, casa în care locuiește să fie
bine aerisită și, dacă e posibil, să doarmă singur în cameră. Dacă tușește, să respecte măsurile igienice,
lucru de alftel valabil pentru toată lumea. Statusul nutrițional se dovedește a fi de mare importanță atât în
ceea ce privește prevenția tuberculozei cât și pentru evoluția bolnavului de tuberculoză. Imunodeficiența
secundară malnutriției crește susceptibilitatea gazdei la infecție. De asemenea, s-a demonstrat că pacienții
bolnavi de tuberculoză malnutriți au o evoluție spre vindecare mai lentă și rate de mortalitate mai mari
decât pacienții hrăniți corespunzător. Astfel, administrarea de suplimente nutritive pot reprezenta o
opțiune pentru o recuperare mai rapidă, iar creșterea statusului nutrițional al populației poate constitui o
măsură eficientă de control a tuberculozei[23]
.
Limitările acestui studiu au fost următoarele:
● lot relativ mic de pacienți, fapt ce poate duce la o supraraportare a reacțiilor adverse la
tratamentul tuberculostatic, potrivit meta-analizei lui Xia YY et al., care a constatat o variație a
incidenței reacțiilor adverse de la 5,5% la 57,8%, în funcție de dimensiunea și proveniența
grupului studiat și definirea reacțiilor adverse, cu o incidență scăzută la studii cu loturi mai
numeroase[24]
;
● studiul este retrospectiv, ceea ce înseamnă că pot lipsi anumite date din foile de observație
precum analize de laborator sau evoluția zilnică completă a pacientului pe durata internării,
documentele fiind analizate la o perioadă de timp după externarea subiecților;
● au existat două cazuri ce nu au primit tratament, un caz infirmat și un caz externat cu
recomandare de inițiere a tratamentului strict supravegheat;
● imposibilitatea de a evalua cu precizie cantitatea de alcool consumată de unii dintre pacienții care
au recunoscut consumul cronic/ocazional de alcool (în consecință, decizia de a-i încadra în lotul
cazurilor de etilism cronic a fost la latitudinea autorilor).

Concluzii
Prin intermediul acestui studiu cantitativ retrospectiv ne-am propus să analizăm corelațiile existente între
variabilele ce țin de pacienți (vârstă, sex, comorbidități asociate) și evoluția și răspunsul acestora la
schemele de tratament cu tuberculostatice, urmărind incidența reacțiilor adverse și modalitățile de
tratament și combatere a acestora.
Rezultatele obținute sunt în concordanță cu cele înregistrate în multiplele studii derulate în cercetarea
tuberculozei. Astfel, într-un lot de 60 de pacienți cu tuberculoză pulmonară și extrapulmonară, cu
predominanța sexului masculin, reacțiile adverse s-au manifestat la 45% din ei. Ele au fost mai frecvente
în rândul pacienților cu vârste mai mari de 60 de ani sau în rândul persoanelor de sex feminin, ceea ce
susține ideea conform căreia vârsta și sexul feminin ar putea fi considerați factori de risc în apariția
reacțiilor adverse la tuberculostatice. Cele mai întâlnite reacții adverse au fost cele de tip hepatic, și
acestea cu predispoziție către sexul feminin, ceea ce constituie o dovada pentru rolul protectiv al sexului
masculin împotriva hepatotoxicității. Prezența comorbidităților, îndeosebi a etilismului cronic, hepatitei
cronice cu virusuri hepatitice B sau C și insuficienței renale cronice, a predispus la manifestarea reacțiilor
adverse.
S-a constatat faptul că evoluția pacienților sub tratament tuberculostatic strict supravegheat pe durata
internării a fost consemnată ca favorabilă sau lent favorabilă în proporție de 94,83%, ridicându-se
premisele unei evoluții asemănătoare și după externare, încheiată prin vindecarea pacienților. Considerăm
astfel că măsurile luate în conformitate cu Programul Național de Control al Tuberculozei tind să aibă o
eficiență crescută, introducerea acestui program conferind planului de eradicare națională a tuberculozei
un caracter realist, cu posibilitatea realizării sale într-o periodă nu foarte îndelungată.
În concluzie, medicamentele antituberculoase administrate în regimuri de tratament au o rată mare de
eficiență, dar și o toxicitate relativă, influențată de vârsta, sexul și comorbiditățile asociate ale pacientului,
reunite sub caracterul de factori de risc ce predispun la reacții adverse. Tratamentul specific acestei
patologii prezintă astfel posibilități de creștere a eficienței prin îmbunătățirea toleranței și scăderea
frecvenței reacțiilor adverse.
Această lucrare este efectuată în cadrul Programului Operațional Sectorial pentru Dezvoltarea Resurselor Umane
(POSDRU), finanțat din Fondul Social European și Guvernul României prin contractul nr.
POSDRU/156/1.2/G/141745.

Bibliografie:
1. Didilescu C, Nicolaescu O. Tuberculoza pulmonară. În Ghiduri de practică medicală, sub red.
Gherasim L., Editura Infomedica, 1999, volumul I, 149-82.
2. Bumbăcea D, Diţiu L, Toma C, Tudose C şi col. Tuberculoza – Curs pentru studenţi, Tipografia
Everest, 2005
3. ***OMS, Geneva. Global Tuberculosis Report 2014
4. Baghaei P, Tabarsi P, Chitsaz E, Saleh M, Marjani M, Shemirani S, Pooramiri MV, Kazempour M,
Farnia P, Fahimi F, Mansouri D, Masjedi M. Incidence, clinical and epidemiological risk factors, and
outcome of drug-induced hepatitis due to antituberculous agents in new tuberculosis cases. Am J Ther.
2010; 17:17–22
5. Resende LSO, dos Santos-Neto ET. Risk factors associated with adverse reactions to antituberculosis
drugs. Jornal Brasileiro de Pneumologia. 2015; 41(1):77-89.
6. Yee D, Valiquette C, Pelletier M, Parisien I, Rocher I, Menzies D. Incidence of serious side effects
from first-line antituberculosis drugs among patients treated for active tuberculosis. Am J Respir Crit
Care Med. 2003; 167(11):1472–1477
7. Lee AM, Mennone JZ, Jones RC, Paul WS. Risk factors for hepatotoxicity associated with rifampin
and pyrazinamide for the treatment of latent tuberculosis infection: experience from three public health
tuberculosis clinics. Int J Tuberc Lung Dis. 2002; 6(11):995–1000.
8. Kim SY, Lee S-M, Yim J-J, et al. Treatment Response and Adverse Reactions in Older Tuberculosis
Patients with Immunocompromising Comorbidities. Yonsei Medical Journal. 2013; 54(5):1227-1233.
doi:10.3349/ymj.2013.54.5.1227.
9. Pande JN, Singh SP, Khilnani GC, Khilnani S, Tandon RK. Risk factors for hepatotoxicity from
antituberculosis drugs: a case-control study. Thorax. 1996; 51(2):132-136.
10. Wong WM, Wu PC, Yuen MF, Cheng CC, Yew WW, Wong PC, Tam CM, Leung CC, Lai CL.
Antituberculosis drug-related liver dysfunction in chronic hepatitis B infection.
Hepatology. 2000 Jan; 31(1):201-6. PubMed PMID: 10613746.
11. Ungo JR, Jones D, Ashkin D, Hollender ES, Bernstein D, Albanese AP, Pitchenik
AE. Antituberculosis drug-induced hepatotoxicity. The role of hepatitis C virus
and the human immunodeficiency virus. Am J Respir Crit Care Med. 1998 Jun; 157(6
Pt 1):1871-6. PubMed PMID: 9620920.
12. Quantrill SJ, Woodhead MA, Bell CE, Hardy CC, Hutchison AJ, Gokal R.
Side-effects of antituberculosis drug treatment in patients with chronic renal
failure. Eur Respir J. 2002 Aug; 20(2):440-3. PubMed PMID: 12212979.
13. Baghaei P, Marjani M, Tabarsi P, Moniri A, Rashidfarrokhi F, Ahmadi F, Nassiri
AA, Masjedi MR, Velayati AA, Cattamanchi A. Impact of chronic renal failure on
anti-tuberculosis treatment outcomes. Int J Tuberc Lung Dis. 2014
Mar; 18(3):352-6. doi: 10.5588/ijtld.13.0726. PubMed PMID: 24670575.

14. Nicolaescu O. Tuberculoza – curs pentru studenți. 2014
15. Vieira DE, Gomes M. Adverse effects of tuberculosis treatment: experience at
an outpatient clinic of a teaching hospital in the city of São Paulo, Brazil. J
Bras Pneumol. 2008 Dec; 34(12):1049-55. English, Portuguese. PubMed PMID:
19180340.
16. Aliasghar Farazi, Masoomeh Sofian, Mansoureh Jabbariasl, and Sara Keshavarz, “Adverse Reactions
to Antituberculosis Drugs in Iranian Tuberculosis Patients,” Tuberculosis Research and Treatment, vol.
2014, Article ID 412893, 6 pages, 2014.
doi:10.1155/2014/412893
17. Obuch-Woszczatyński P, Dubiel G, Harmanus C, et al. Emergence ofClostridium difficile infection in
tuberculosis patients due to a highly rifampicin-resistant PCR ribotype 046 clone in Poland. European
Journal of Clinical Microbiology & Infectious Diseases. 2013; 32(8):1027-1030. doi: 10.1007/s10096-
013-1845-5.
18. Lee YM, Huh KC, Yoon SM, Jang BI, Shin JE, Koo HS, Jung Y, Kim SH, Moon HS,
Lee SW; Daejeon-Chungchung Intestinal Research Group. Incidence and Clinical
Outcomes of Clostridium difficile Infection after Treatment with Tuberculosis
Medication. Gut Liver. 2015 Aug 11. doi: 10.5009/gnl14435.
19. Castro AT, Mendes M, Freitas S, Roxo PC. Incidence and risk factors of major
toxicity associated to first-line antituberculosis drugs for latent and active
tuberculosis during a period of 10 years. Rev Port Pneumol (2006). 2015
May-Jun; 21(3):144-50.
20. Snider DE Jr. Pyridoxine supplementation during isoniazid therapy. Tubercle.
1980 Dec; 61(4):191-6. Review. PubMed PMID: 6269259.
21. Tuberculosis Chemotherapy Centre. The prevention and treatment of isoniazid toxicity in the therapy
of pulmonary tuberculosis: 2. An assessment of the prophylactic effect of pyridoxine in low dosage.
Bulletin of the World Health Organization. 1963; 29(4):457-481.
22. Solangi GA, Zuberi BF, Shaikh S, Shaikh WM. Pyrazinamide induced hyperuricemia
in patients taking anti-tuberculous therapy. J Coll Physicians Surg Pak. 2004
Mar; 14(3):136-8. PubMed PMID: 15228843. Xia YY, Hu DY, Liu FY, et al. Design of the Anti-
tuberculosis Drugs induced Adverse Reactions in China National Tuberculosis Prevention and Control
Scheme Study (ADACS). BMC Public Health. 2010; 10:267. doi: 10.1186/1471-2458-10-267.
23. Gupta KB, Gupta R, Atreja A, Verma M, Vishvkarma S. Tuberculosis and nutrition. Lung India :
Official Organ of Indian Chest Society. 2009; 26(1):9-16. doi:10.4103/0970-2113.45198.
24. Xia YY, Hu DY, Liu FY, et al. Design of the Anti-tuberculosis Drugs induced Adverse Reactions in
China National Tuberculosis Prevention and Control Scheme Study (ADACS). BMC Public Health.
2010; 10:267. doi: 10.1186/1471-2458-10-267.